Gli stati di aggregazione della materia
Che cosa sono gli stati di aggregazione della materia? E quali sono?
La materia è formata da particelle di vario tipo. In base alla distanza tra le particelle e alla loro libertà di movimento, essa può presentarsi in tre stati diversi, chiamati stati di aggregazione:
- stato solido, come la roccia
- stato liquido, come l’acqua
- stato aeriforme, come l’aria
Lo stato solido
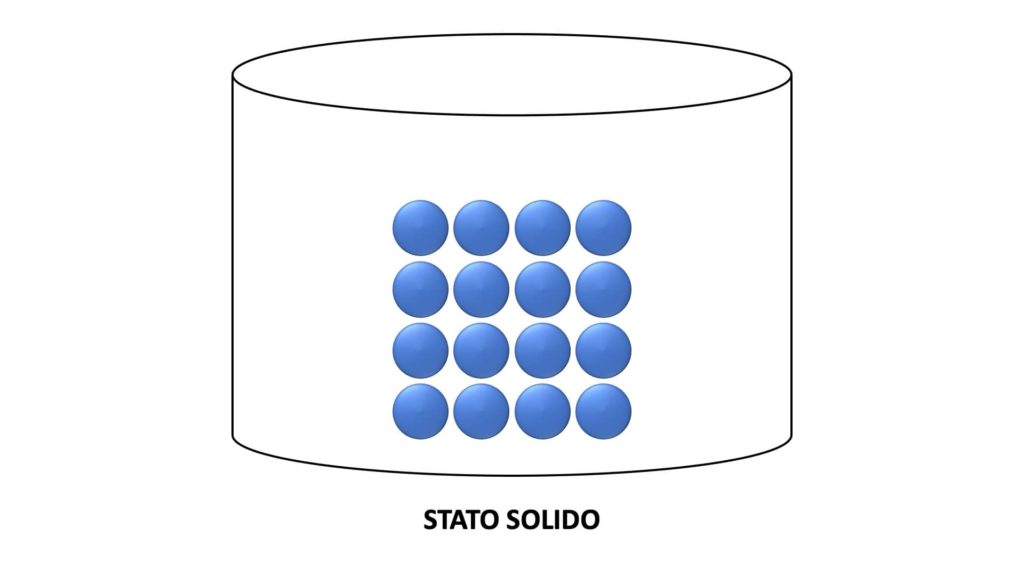
La materia allo stato solido ha volume proprio e forma propria. Ad esempio, un sasso occupa un volume ben preciso e ha una forma ben precisa.
In questo stato le particelle sono legate da forze molto intense e pertanto non possono muoversi liberamente, ma solo vibrare (questo movimento prende il nome di moto vibrazionale):
Lo stato liquido
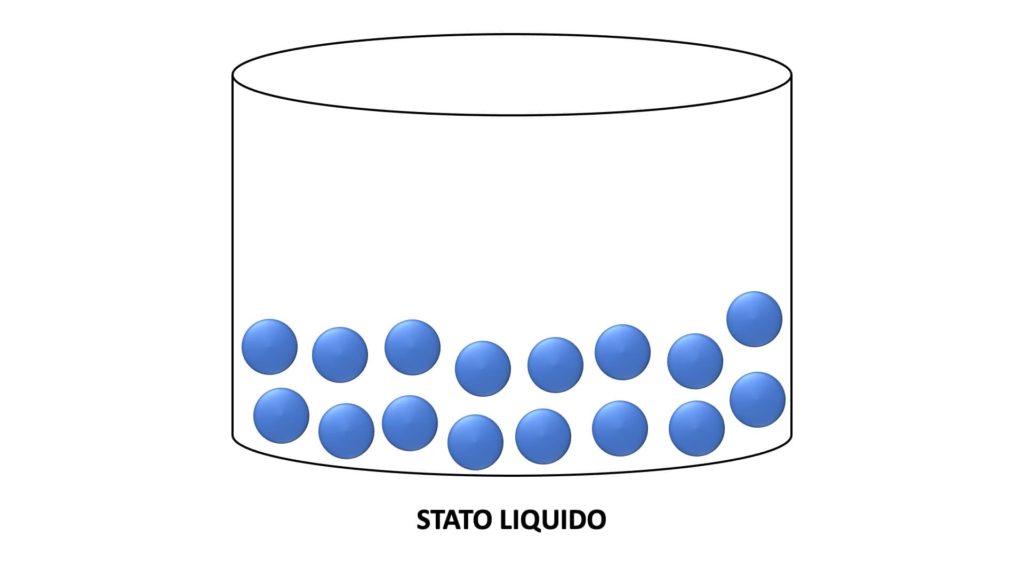
La materia allo stato liquido ha volume proprio e assume la forma del recipiente che la contiene. Ad esempio, un litro d’acqua occupa un volume ben preciso, ma cambia forma a seconda che venga versato in una bottiglia, in una pentola o in una damigiana.
Le particelle sono legate da forze meno intense rispetto ai solidi, per cui possono scorrere l’una sull’altra:
Lo stato aeriforme
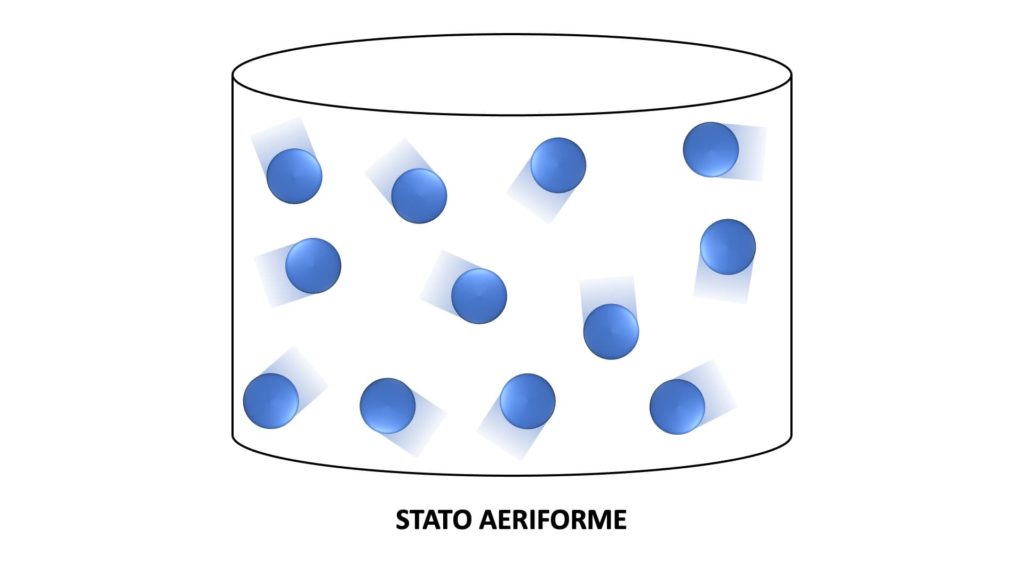
La materia allo stato aeriforme non ha né volume proprio né forma propria. Le particelle infatti, che presentano legami debolissimi e possono quindi muoversi liberamente, tendono a espandersi il più possibile, occupando così tutto il volume disponibile e assumendo la forma del recipiente:
Le proprietà degli stati di aggregazione
I solidi hanno una densità alta, i liquidi una densità media e gli aeriformi una densità bassa.
Inoltre, i solidi e i liquidi sono incomprimibili, mentre gli aeriformi sono comprimibili (in altre parole, se i solidi o i liquidi vengono sottoposti a una qualsiasi pressione, il loro volume non diminuisce, mentre quello degli aeriformi sì).
Ecco una tabella riassuntiva delle proprietà di ciascuno stato:
| Volume | Forma | Particelle | Densità | Effetto della pressione | |
| Solidi | Proprio | Propria | Vicine e ordinate | Alta | Incomprimibili |
| Liquidi | Proprio | Forma del recipiente | Vicine e disordinate | Media | Incomprimibili |
| Aeriformi | Occupa tutto il volume disponibile | Forma del recipiente | Distanti e disordinate | Bassa | Comprimibili |
Stati di aggregazione e passaggi di stato
Gli stati di aggregazione della materia non sono una caratteristica fissa. Se la temperatura o la pressione variano, la materia può passare da uno stato all’altro.
L’acqua ad esempio è liquida, ma può diventare solida (ghiaccio) o aeriforme (vapore acqueo).
Queste trasformazioni prendono il nome di passaggi di stato:
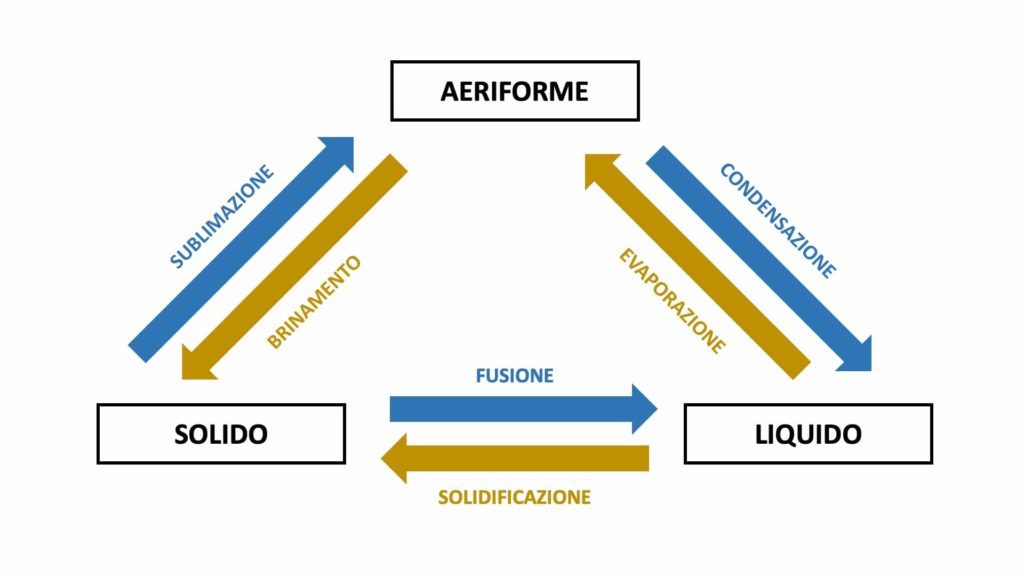
- solidificazione = da liquido a solido
- fusione = da solido a liquido
- evaporazione = da liquido ad aeriforme
- condensazione = da aeriforme a liquido
- brinamento = da aeriforme a solido
- sublimazione = da solido ad aeriforme
Ecco uno schema riassuntivo dei vari passaggi di stato:
Come si comportano le particelle al variare della temperatura o della pressione?
Se la temperatura aumenta, aumenta anche l’energia cinetica delle particelle, che iniziano quindi a muoversi più liberamente e a rompere in questo modo i legami che le uniscono. Viceversa, se la temperatura diminuisce, diminuisce anche l’energia cinetica delle particelle, che iniziano così ad avvicinarsi le une alle altre e a legarsi tra loro.
Se la pressione aumenta, diminuisce lo spazio in cui possono muoversi le particelle, che iniziano quindi ad avvicinarsi le une alle altre e a legarsi tra loro. Viceversa, se la pressione diminuisce, aumenta lo spazio in cui possono muoversi le particelle, che iniziano così ad allontanarsi le une dalle altre e a rompere i legami che le uniscono.
Per sapere a quale temperatura e a quale pressione corrispondono gli stati di aggregazione di una sostanza, si usa il cosiddetto diagramma di stato.
Lo stato plasmatico
Oltre allo stato solido, liquido e aeriforme, esiste anche un quarto stato di aggregazione, lo stato plasmatico, che corrisponde a un gas ionizzato, cioè a un gas formato da ioni ed elettroni.
Di solito questo stato non viene studiato a scuola perché non è presente sulla Terra (lo troviamo ad esempio nelle stelle).
